Dra.MSc.Ibis Alexandra Orejuela Escobar
PRÓLOGO
El llevar a cabo este estudio en el marco del Máster Universitario de Valoración de Daño Corporal y Peritaje Médico 2017-2019, me ha permitido profundizar en la temática de las dolencias cardíacas, básicamente isquémicas y su repercusión en el ámbito del trabajo.
Es todo lo relacionado con el mundo laboral, lo que me ha motivado a investigar, tanto la faceta médica y pericial dentro de la patología forense cardíaca como su repercusión a nivel de los Tribunales, cuyas sentencias vienen a clarificar si se puede o no catalogar de “accidente laboral”, o que el trabajador sea subsidiario de Incapacidad Permanente.
ATEROESCLEROSIS
La aterosclerosis es la primera causa de mortalidad y morbilidad en las naciones desarrolladas. Por efecto de sus manifestaciones principales (el infarto de miocardio y el evento vascular cerebral) también se ha convertido en una causa importante de muerte en el mundo en desarrollo.
Conocida a menudo como endurecimiento de las arterias, la palabra aterosclerosis proviene de las raíces griegas atheros, que significa papilla grumosa y skleros, que significa duro.
La evidencia reciente demostró que la inflamación crónica desencadena el proceso ateroscleroso y traduce los factores de riesgo tradicionales (por ejemplo, la hipercolesterolemia) en un comportamiento anómalo de las células de la pared vascular, lo que contribuye a la enfermedad y a sus complicaciones trombóticas. La aterosclerosis puede evolucionar en un estado de latencia durante la edad adulta, que se ve interrumpido por eventos cardiovasculares agudos.

COMPLICACIONES DE LA ATEROSCLEROSIS
Las placas aterosclerosas no muestran distribución homogénea en la vasculatura. Suelen desarrollarse primero en la cara dorsal de la aorta abdominal y en los segmentos proximales de las arterias coronarias, seguidos por las arterias poplíteas, la aorta descendente torácica, las arterias carótidas internas y las arterias renales. Por lo tanto, las regiones irrigadas por estos vasos sufren con más frecuencia las consecuencias de la aterosclerosis.
Las complicaciones de las placas aterosclerosas –incluidas calcificación, rotura, hemorragia y embolia- pueden tener consecuencias clínicas directas por efecto de la restricción aguda del flujo sanguíneo o las alteraciones de la integridad de la pared vascular. Estas complicaciones, comprenden las siguientes:
- Calcificación de la placa aterosclerosa, capaz de incrementar su fragilidad.
- Rotura o ulceración de la placa aterosclerosa, que expone a los procoagulantes contenidos en la placa a la sangre circulante, lo que genera la formación del trombo en ese sitio. Este tipo de trombosis puede ocluir el vaso y producir un infarto en el órgano afectado. De manera alternativa, el trombo puede organizarse, incorporarse a la lesión e incrementar el volumen de la placa.
- Hemorragia dentro de la placa derivada de la rotura de la cubierta fibrosa o de la microvasculatura que se forma dentro de la lesión. El hematoma intramural resultante puede limitar aún más el lumen del vaso.
- Embolia de fragmentos de ateroma destruido hacia regiones vasculares distales.
- Debilitamiento de la pared vascular: la placa fibrosa somete a la capa media colindante a una mayor presión, que puede originar la atrofia y la pérdida del tejido elástico, con expansión subsecuente de la arteria y la formación de un aneurisma.
- Desarrollo de microvasos dentro de la placa, que constituyen una fuente de hemorragia intraplaca y favorecen el tráfico de leucocitos.
Las complicaciones de la placa aterosclerosa pueden traer consigo consecuencias clínicas específicas en distintos sistemas orgánicos. Cuando el crecimiento de la lesión rebasa de manera eventual la dilatación compensadora de la placa, la lesión puede restringir el lumen vascular y, de tratarse de las arterias coronarias, producir malestar precordial intermitente durante el ejercicio (angina de pecho).
En contraste, la placa que no compromete el lumen vascular pero tiene características de vulnerabilidad (p.ej., una cubierta fibrosa delgada, un núcleo lipídico grande, calcificaciones puntiformes) puede romperse, lo que determina una trombosis aguda y un infarto de miocardio. Estas placas no estenosantes son con frecuencia numerosas y se encuentran diseminadas en el árbol arterial, y puesto que no limitan el flujo arterial no provocan síntomas y a menudo escapan a la detección mediante pruebas de esfuerzo o angiografía.
La descripción que se presenta aquí de la aterogénesis y sus complicaciones permite explicar las limitaciones de ciertos tratamientos de amplio uso. Por ejemplo, la intervención percutánea (angioplastia y colocación de stent) de las estenosis coronarias sintomáticas alivia de modo efectivo la angina de pecho, pero no necesariamente previene el infarto de miocardio a futuro o prolonga la vida, con excepción de los pacientes que se encuentran en la fase inicial de un infarto agudo de miocardio con elevación del segmento ST. Es probable que esta disparidad sea un reflejo de las numerosas placas no oclusivas en riesgo de precipitar eventos trombóticos. Esto se traduce en que las modificaciones del estilo de vida y los tratamientos farmacológicos que modifican los factores de riesgo para la formación de la placa, y limitan las características relacionadas con la vulnerabilidad, constituyen un fundamento crucial para prevenir el avance y las complicaciones de la ateroesclerosis.
FACTORES DE RIESGO PARA LA ATEROESCLEROSIS
En los primeros años del siglo XX casi todos consideraban a la aterosclerosis como un proceso inevitable del envejecimiento. Sin embargo, en 1948 la emblemática investigación Framingham Heart Study comenzó a analizar la relación entre atributos específicos y la enfermedad cardiovascular, y se estableció el concepto de factores de riesgo ateroscleroso.
Entre los factores de riesgo principales, los que no son susceptibles de corrección son la edad avanzada, el sexo masculino y la herencia –es decir, el antecedente de cardiopatía coronaria en parientes en primer grado a edad temprana (antes de los 55 años en un pariente varón o de los 65 años en un pariente mujer)-. Los factores de riesgo para aterosclerosis sensibles de modificación incluyen las concentraciones y los perfiles inapropiados de lípidos circulantes (dislipidemias), el tabaquismo, la hipertensión, la diabetes mellitus, el sedentarismo y la obesidad.
Además de estos factores predictivos estándar, ciertos marcadores biológicos relacionados con el desarrollo de eventos cardiovasculares han sido sometidos a una evaluación rigurosa como marcadores de riesgo novedosos. Entre ellos se encuentran las concentraciones circulantes altas de la partícula lipoproteica especial Lp(a) y ciertos marcadores de inflamación, entre otros la proteína C reactiva (PCR), un reactante de la fase aguda. Por otro lado, estudios de asociación en el genoma (EAG) recientes han tratado de identificar variantes de locus genéticos asociados con el incremento de riesgo cardiovascular.
Las secciones siguientes hacen referencia a estos factores de riesgo y marcadores biológicos.
GENÉTICA
La predisposición genética, que revela los antecedentes familiares, constituye un factor de riesgo importante para la aterosclerosis. Aunque no se han podido detectar genes causales de manera directa, estudios de la asociación en el genoma recientes identificaron distintos locus vinculados con la enfermedad aterosclerosa.
La conexión más intensa con la arteriopatía coronaria y el infarto de miocardio se relaciona con la región cromosómica 9p21.3. Esta región contiene genes que codifican dos inhibidores de cinasas dependientes de ciclina capaces de regular el ciclo celular y que pudieran participar en las vías de inhibición del TGF-B.
Estos hallazgos y otros prometen favorecer de manera eventual la identificación, la prevención y el tratamiento de la enfermedad ateroesclerosa.
FACTORES DE RIESGO TRADICIONALES
DISLIPEMIAS
Un gran y congruente cuerpo de evidencia define las concentraciones anómalas de lípidos circulantes como un factor de riesgo importante para la aterosclerosis.
Estudios de observación han demostrado que las sociedades con consumo abundante de grasas saturadas y mayor prevalencia de hipercolesterolemia tienen una mortalidad más alta por coronariopatía que los países con un consumo tradicional limitado de grasas saturadas y concentraciones séricas bajas de colesterol (p.ej., regiones rurales de Japón y ciertas naciones mediterráneas). De manera similar, datos del Framingham Heart Study y otras cohortes han demostrado que el riesgo de cardiopatía isquémica se incrementa a la par de las concentraciones más altas de colesterol sérico total. El riesgo coronario casi se duplica en una persona con una concentración total de colesterol de 240 mg/dl en comparación con un individuo cuya concentración de colesterol es de 200 mg/dl.
En particular, las concentraciones altas de LDL circulante se correlacionan con un aumento de la incidencia de aterosclerosis y arteriopatía coronaria. Cuando están en concentraciones excesivas, las LDL pueden acumularse en el espacio subendotelial y sufrir modificaciones químicas que dañan en mayor medida la íntima, como se describe antes, lo que da inicio y perpetúa el desarrollo de las lesiones aterosclerosas.
Así, las LDL, se conocen por lo general como colesterol malo. Por el contrario, una concentración elevada de partículas de HDL (con frecuencia denominadas colesterol bueno) se vincula con la protección contra la aterosclerosis, muchas veces atribuida a la capacidad de estas partículas para transportar el colesterol desde los tejidos periféricos hasta el hígado para su eliminación (lo que se denomina transporte inverso de colesterol), así como a las propiedades antioxidantes y antiinflamatorias que se les atribuyen.
La elevación de las concentraciones séricas de LDL pueden persistir por muchas razones, lo que incluye una dieta rica en grasas o anomalías del mecanismo de eliminación del receptor de las LDL. Los pacientes con defectos genéticos del receptor de las LDL, que desencadenan una afección llamada hipercolesterolemia familiar, no pueden eliminar estas partículas de la circulación con eficacia.
Evidencia creciente también implica a las lipoproteínas ricas en triglicéridos, entre éstas las VLDL y las IDL, en el desarrollo de la aterosclerosis. Sin embargo, queda por determinar si estas partículas participan de manera directa en la enfermedad o tan sólo acompañan a las concentraciones bajas de colesterol en HDL. Debe señalarse que la diabetes mellitus tipo 2 mal controlada se asocia a menudo con la combinación de hipertrigliceridemia y concentraciones bajas de HDL.
Terapia modificadora de los lípidos
Las estrategias que mejoran las concentraciones anómalas de lípidos pueden limitar las complicaciones de la aterosclerosis. Muchos estudios grandes con pacientes con coronariopatía confirman que la disminución del colesterol sérico por medios dietéticos o farmacológicos permite prevenir eventos cardiovasculares.
Las modificaciones del estilo de vida que pudieran ser benéficas incluyen evitar el tabaquismo, el mantenimiento de una dieta y un peso saludables, así como el incremento de la actividad física. Pero incluso una modificación intensiva del estilo de vida puede no ser suficiente para prevenir los efectos cardiovasculares en individuos con factores de riesgo ateroscleroso de larga evolución. Por ende, muchas personas requieren agentes farmacológicos para optimizar su evolución cardiovascular.
Los principales grupos de fármacos modificadores de los lípidos incluyen los inhibidores de la reductasa de la HMG-CoA (también llamados estatinas), la niacina, los derivados del ácido fíbrico, los inhibidores de la absorción intestinal del colesterol y los agentes quelantes de los ácidos biliares.
Entre éstos, las estatinas han surgido como los fármacos clave para la disminución de las LDL, capaces de disminuir los eventos cardiovasculares en una gran diversidad de pacientes. Estos agentes inhiben a la enzima limitante de la velocidad de la biosíntesis del colesterol. La disminución resultante de la concentración intracelular de colesterol favorece una mayor expresión del receptor de las LDL y, con ello, aumenta el retiro de las partículas de LDL del torrente sanguíneo. Las estatinas también disminuyen la velocidad de síntesis de las VLDL en el hígado (con lo que reducen las concentraciones de triglicéridos circulantes) y elevan las HDL por un mecanismo desconocido.
Estudios clínicos importantes que evaluaron el tratamiento con estatinas demostraron disminución tanto de eventos cardíacos isquémicos, como en la incidencia de eventos vasculares cerebrales isquémicos y las tasas de mortalidad en individuos con y sin antecedente de eventos cardiovasculares aterosclerosis.
TABAQUISMO
Numerosos estudios han demostrado que el tabaquismo predispone a la aterosclerosis y a la cardiopatía isquémica. Incluso el tabaquismo de bajo nivel determina una evolución adversa, pero quienes muestran un consumo más intenso tienen un riesgo más alto de eventos cardiovasculares.
El tabaquismo podría promover la enfermedad ateromatosa por distintas vías, lo que incluye una mayor modificación oxidativa de las LDL, la disminución de las concentraciones circulantes de HDL, la disfunción endotelial derivada de la hipoxia tisular y el incremento del estrés oxidativo, el aumento de la adhesividad plaquetaria, el aumento de la expresión de MAL solubles, la estimulación inapropiada del sistema nervioso simpático por la nicotina, y el desplazamiento del oxígeno de la hemoglobina por efecto del monóxido de carbono.
La extrapolación a partir de experimentos en animales sugiere que el tabaquismo no sólo acelera la aterogénesis, sino que también intensifica la propensión a la trombosis –ambas componentes del paciente vulnerable.
Por fortuna la supresión del tabaquismo puede revertir ciertas evoluciones adversas. Las personas que dejan de fumar reducen en gran medida su riesgo de cursar con cardiopatía coronaria, en comparación con quienes continúan fumando. En un estudio, después de 3 años de abandonar el tabaquismo, el riesgo de arteriopatía coronaria entre individuos con antecedente de tabaquismo adquirió valores similares al de sujetos que nunca habían fumado.
HIPERTENSIÓN
La presión arterial alta (ya sea sistólica o diastólica) aumenta el riesgo de desarrollar aterosclerosis, arteriopatía coronaria y evento vascular cerebral. La relación entre la presión arterial elevada y la enfermedad cardiovascular no parece tener un umbral específico. Más bien, el riesgo se incrementa de modo continuo ante valores de presión que crecen progresivamente. La presión sistólica predice una evolución adversa de manera más confiable que la presión diastólica, en particular en personas mayores.
La hipertensión puede acelerar la aterosclerosis por distintas vías. Estudios en animales han demostrado que la presión arterial elevada lesiona el endotelio vascular y puede incrementar la permeabilidad de la pared vascular a las lipoproteínas. La angiotensina II, una mediadora de la hipertensión, actúa no sólo como vasoconstrictor sino también como estimulante del estrés oxidativo. Así, la hipertensión también puede promover la aterogénesis al contribuir al estado oxidativo e inflamatorio.
Terapia antihipertensiva
Al igual que para las dislipemias, el tratamiento de la hipertensión debe comenzar con modificaciones del estilo de vida, pero a menudo requiere la intervención farmacológica. Los estudios Dietary Approaches to Stop Hypertension (DASH) demostraron que una dieta rica en frutas y verduras, con productos lácteos bajos en grasa y un contenido general bajo en sodio, mejora en grado significativo las presiones arteriales sistólica y diastólica. El ejercicio practicado con regularidad también puede disminuir las cifras de presión arterial en reposo. Muchos medicamentos disminuyen en forma efectiva la presión arterial (diuréticos, simpaticolíticos, vasodilatadores y antagonistas del sistema renina-angiotensina-aldosterona).
DIABETES MELLITUS Y SÍNDROME METABÓLICO
La diabetes mellitus afecta a cerca de 170 millones de personas en todo el mundo, una prevalencia que se espera crecerá un 40% para el 2030. Con el incremento de tres a cinco veces del riesgo de eventos coronarios agudos, el 80% de los pacientes diabéticos mueren por afecciones relacionadas con la aterosclerosis, lo que incluye la cardiopatía coronaria, el evento vascular cerebral y la arteriopatía periférica.
La predisposición de los pacientes diabéticos a la aterosclerosis puede guardar relación en parte con la dislipemia concomitante, la glucosilación no enzimática de las lipoproteínas (que fomenta la retención de colesterol en los macrófagos de captura), la tendencia protrombótica asociada y el estado antifibrinolítico. El tratamiento de la hipertensión y la dislipemia en individuos diabéticos, reduce de manera convincente el riesgo de complicaciones cardíacas y cerebrovasculares.
El síndrome metabólico (también llamado síndrome de resistencia a la insulina) hace referencia a un cúmulo de factores de riesgo, al que pertenecen la hipertensión, la hipertrigliceridemia, la disminución de las HDL, la hiperglucemia y la obesidad visceral (exceso de tejido adiposo en la región abdominal). Esta constelación se relaciona con un riesgo mayor de aterosclerosis lo mismo en pacientes diabéticos que no diabéticos. La presencia de resistencia a la insulina en este síndrome parece favorecer la aterogénesis mucho tiempo antes de que la persona afectada desarrolle diabetes franca.
SEDENTARISMO
El ejercicio puede mitigar la aterogénesis por varias vías. Además de sus efectos benéficos sobre el perfil lipídico y la presión arterial, el ejercicio fomenta la sensibilidad a la insulina. Estudios de observación tanto en hombres como en mujeres indican que incluso actividades modestas, -por ejemplo la caminata rápida, por un período limitado de 30 minutos al día- confieren protección contra la mortalidad cardiovascular.
CONDICIÓN ESTROGÉNICA
Antes de la menopausia las mujeres tienen una incidencia menor de eventos coronarios que los hombres. Sin embargo, después de la menopausia las mujeres muestran tasas similares a las de los hombres. Esta observación sugiere que los estrógenos (cuyas concentraciones declinan tras la menopausia) pueden tener propiedades ateroprotectoras. Las concentraciones fisiológicas de estrógenos en las mujeres premenopáusicas incrementan las HDL y reducen las LDL. Desde la perspectiva experimental, los estrógenos también tienen acciones antioxidantes y antiagregantes potencialmente benéficas y mejoran la vasodilatación dependiente del endotelio.
BIOMARCADORES DEL RIESGO CARDIOVASCULAR
Pese a la identificación de los bien definidos factores de riesgo recién descritos, uno de cada cinco eventos cardiovasculares ocurre en individuos que carecen de estos atributos. Junto con el conocimiento creciente sobre la patogenia de la aterosclerosis, han surgido varios marcadores de riesgo novedosos. Estos biomarcadores desempeñan tres papeles principales: Como medio para facilitar la estratificación del riesgo para la enfermedad ateroesclerosa y orientar así la selección del tratamiento, como medida clínica para valorar los efectos terapéuticos y blancos potenciales de regímenes terapéuticos nuevos.
LIPOPROTEÍNA (A)
La lipoproteína (a), conocida como Lp (a), predice de manera independiente los eventos cardiovasculares en algunos estudios.
La Lp (a) es capaz de ingresar a la íntima arterial, y estudios in vitro han demostrado que impulsa la inflamación y la trombosis.
PROTEÍNA C REACTIVA Y MARCADORES DE INFLAMACIÓN
Toda vez que la patogenia de la aterosclerosis implica inflamación en cada una de sus fases, los marcadores inflamatorios se han sometido a evaluación como factores predictivos del riesgo cardíaco.
Estudios importantes en hombres y mujeres aparentemente sanos indican que en quienes cuentan con concentraciones iniciales mayores de PCR, el riesgo de una evolución cardiovascular adversa aumenta, en forma independiente a las concentraciones séricas de colesterol y otros marcadores de riesgo tradicionales.
Numerosos estudios prospectivos afirman que la PCR cuantificada mediante un ensayo con sensibilidad alta, predice de manera independiente infarto de miocardio, evento vascular cerebral, arteriopatía periférica y muerte súbita de origen cardíaco.
Dado el papel crucial de la inflamación en la aterogénesis, estudios clínicos activos están probando fármacos antiinflamatorios disponibles y novedosos para la prevención de los eventos cardiovasculares recurrentes en individuos con coronariopatía.
CARDIOPATÍA ISQUÉMICA
En 1772, el médico británico William Heberden informó un trastorno en el que los pacientes desarrollaban una sensación desagradable en la región precordial al caminar. Lo denominó angor pectoris. Heberden observó que este malestar desaparecía poco después de que el paciente dejara de caminar, pero reincidía con actividades similares. Si bien desconocía su causa, es probable que fuera el primero en describir los síntomas de la cardiopatía isquémica, condición en que existe un desequilibrio entre el aporte y la demanda de oxígeno en el miocardio, casi siempre derivada de la aterosclerosis de las arterias coronarias.
Definiciones clínicas
Cardiopatía isquémica
– Condición en la que existe desequilibrio entre el aporte y la demanda de oxígeno en el miocardio, que trae consigo hipoxia miocárdica y acumulación de metabolitos de desecho, casi siempre generada por enfermedad aterosclerosa en las arterias coronarias (a menudo denominada arteriopatía coronaria).
Angina de pecho (angor pectoris)
– Sensación incómoda en el tórax y las estructuras anatómicas vecinas, inducida por la isquemia de miocardio.
Angina estable
– Patrón crónico de angina de pecho transitoria, precipitada por la actividad física o la inquietud emocional, que se alivia con el reposo en el transcurso de algunos minutos; los episodios a menudo se relacionan con una depresión temporal del segmento ST, pero no se produce daño miocárdico permanente.
Angina variante
– Malestar anginoso típico, por lo general en reposo, que se desarrolla por un espasmo arterial coronario más que por un incremento de la demanda de oxígeno en el miocardio; los episodios suelen asociarse con desplazamientos transitorios del segmento ST, por lo general elevación (también denominada angina de Prinzmetal).
Isquemia silente
– Episodios asintomáticos de isquemia miocárdica; pueden detectarse mediante electrocardiografía y otras técnicas de gabinete.
Angina inestable
– Patrón de incremento de frecuencia y duración de los episodios anginosos, que ocurren con un esfuerzo físico menor o en reposo; a menudo evoluciona al infarto de miocardio si no se recibe tratamiento.
Infarto de miocardio
– Región de necrosis miocárdica que suele derivar de la suspensión prolongada de la irrigación sanguínea; casi siempre deriva de la formación aguda de un trombo en un punto de estenosis ateroesclerosa coronaria; puede ser la primera manifestación clínica de la cardiopatía isquémica o puede ir precedido por el antecedente de angina de pecho.
CARACTERÍSTICAS CLÍNICAS DE LA ANGINA ESTABLE CRÓNICA
Anamnesis
El componente más importante de la evaluación clínica de la cardiopatía isquémica son los antecedentes referidos por el paciente. Puesto que el dolor torácico es un síntoma común, es primordial concentrarse en las características que ayudan a diferenciar la isquemia miocárdica de otras causas de malestar.
Calidad
La angina se describe casi siempre como una sensación de presión, malestar, opresión, ardor o pesadez en la región precordial. Es raro que la sensación de hecho se describa como dolor.
En ocasiones la persona compara la sensación con la de un elefante que se sienta sobre el pecho. El malestar anginoso no es agudo o cortante, y no varía en gran medida con la inspiración o el movimiento de la pared torácica. Se trata de un malestar constante que dura algunos minutos, rara vez más de 5 a 10. Siempre dura más que algunos segundos, y esto facilita su diferenciación de los dolores musculoesqueléticos más agudos y breves.
Al describir la angina el paciente puede colocar el puño sobre su esternón, denominado signo de Levine, para tratar de definir el malestar constrictivo mediante un empuñamiento firme.
Localización
El malestar anginoso suele ser difuso más que localizarse en un solo punto. Con más frecuencia se localiza en la región retroesternal o en el lado izquierdo de la región precordial, pero suele ubicarse en cualquier sitio del pecho, la espalda, los brazos, el cuello, el segmento inferior de la cara o el hemiabdomen superior. En muchas ocasiones se irradia hacia los hombros y la cara interna de los brazos, en particular en el lado izquierdo.
Síntomas acompañantes
Durante el malestar de un cuadro anginoso agudo, la estimulación simpática y parasimpática generalizada puede traer consigo taquicardia, diaforesis y náusea. También son comunes la fatiga y la debilidad transitorias, en particular en pacientes ancianos.
Desencadenantes
La angina, cuando no deriva del vasoespasmo puro, es precipitada por condiciones que incrementan la demanda miocárdica de oxígeno (p.ej., el aumento de la frecuencia cardíaca, la contractilidad o el estrés parietal). Influyen el esfuerzo físico, la ira y otros tipos de excitación emocional. Factores adicionales que aumentan la demanda miocárdica de oxígeno y pueden precipitar el malestar anginoso, son el consumo abundante de alimentos o el clima frío. Este último induce vasoconstricción periférica, que a su vez aumenta el estrés parietal miocárdico, toda vez que el ventrículo se contrae contra una mayor resistencia.
La angina suele aliviarse en el transcurso de minutos tras suspender la actividad que la precipita, e incluso con mayor rapidez (en el transcurso de 3 a 5 minutos ) mediante el uso de nitroglicerina sublingual. Esta respuesta puede ayudar a diferenciar la isquemia del miocardio de muchos otros trastornos que inducen malestar torácico.
Frecuencia
Si bien el grado de ejercicio necesario para precipitar la angina puede permanecer bastante constante, la frecuencia de los episodios varía en grado considerable, toda vez que los individuos aprenden con rapidez que actividades les generan malestar y las evitan. Por lo tanto es importante interrogar en torno a la disminución de las actividades de la vida cotidiana al integrar la historia clínica.
Factores de riesgo
Además de la descripción del malestar torácico, un interrogatorio cuidadoso debe identificar factores de riesgo que predisponen a la aterosclerosis y la angina, entre otros tabaquismo, dislipemia, hipertensión, diabetes y antecedentes familiares de coronariopatía prematura.
Diagnóstico diferencial
Varios trastornos pueden desencadenar síntomas que se asemejan al malestar precordial transitorio de la angina de pecho, como algunos de origen cardíaco (p.ej., pericarditis), gastrointestinal (p.ej., reflujo gastroesofágico, enfermedad ácido péptica, espasmo esofágico o cólico biliar) y musculoesquelético (incluidos el dolor de la pared torácica, la osteoartritis raquídea y la radiculitis cervical).
El interrogatorio aún es de suma importancia para diferenciar la isquemia del miocardio de estos trastornos. En contraste con la angina de pecho, los trastornos gastrointestinales que generan dolor torácico recurrente a menudo son precipitados por ciertos alimentos y no están relacionados con el ejercicio. El malestar torácico de origen musculoesquelético tiende a ser más superficial o puede localizarse en un sitio definido (es decir, el paciente puede señalar el lugar en que se localiza el dolor con un dedo) y a menudo varía con los cambios de posición. De manera similar, la presencia de dolor de tipo pleurítico (dolor agudo que se intensifica con el movimiento respiratorio) es un argumento en contra de la angina como causa; este síntoma tiene más probabilidad de derivar de la pericarditis, o de algún trastorno pulmonar agudo como la embolia pulmonar o un neumotórax.
Exploración física
Si es posible explorar a una persona durante un cuadro de angina, pueden detectarse varios signos transitorios. Son frecuentes el incremento de la frecuencia cardíaca y la presión arterial debido a que se intensifica la respuesta simpática. La isquemia miocárdica puede desencadenar la disfunción de los músculos papilares e inducir así insuficiencia mitral.
La exploración física también debe descartar signos de enfermedad aterosclerosa en los lechos vasculares más accesibles. Por ejemplo, los soplos carotídeos pueden revelar la presencia de enfermedad cerebrovascular, en tanto los soplos en la arteria femoral o la disminución de los pulsos en las extremidades inferiores pueden ser una clave para identificar la arteriopatía periférica.
Estudios diagnósticos
Una vez que se sospecha la angina, varios procedimientos diagnósticos pueden resultar útiles para confirmar la isquemia del miocardio como la causa. Puesto que muchas de estas pruebas son costosas es importante elegir los estudios más apropiados para cada paciente.
Electrocardiograma
Uno de los instrumentos más útiles es el electrocardiograma obtenido durante el cuadro de angina. Si bien es fácil de obtener cuando los síntomas ocurren el pacientes hospitalizados, puede no ser posible registrar los episodios en las personas que se atienden en servicios ambulatorios.
Durante la isquemia de miocardio pueden aparecer cambios en el segmento ST y la onda T.
Pruebas de esfuerzo
Puesto que los electrocardiogramas que se obtienen durante o entre episodios de malestar precordial pueden ser normales, estos registros no excluyen la cardiopatía isquémica subyacente. Por esta razón, las pruebas de esfuerzo con ejercicio o farmacológicas son auxiliares diagnósticos y pronósticos valiosos.
Prueba estandarizada de esfuerzo
En esta prueba el paciente se ejercita en una banda sin fin o una bicicleta estacionaria con cargas de trabajo progresivamente mayores, y se vigila el desarrollo de malestar precordial o disnea excesiva. Se mantiene un monitoreo continuo de la frecuencia cardíaca y el electrocardiograma, y la presión arterial se verifica a intervalos regulares. La prueba continúa hasta que se desarrolle angina, aparezcan signos de isquemia miocárdica en el electrocardiograma, se alcance una frecuencia cardíaca objetivo o el paciente esté demasiado fatigado para continuar.
La prueba se considera anormal si se reproduce el malestar precordial típico del enfermo o si se desarrollan anomalías congruentes con isquemia en el electrocardiograma.
Estudios de imagenología nuclear
Durante una prueba de imagen de perfusión miocárdica de este tipo se inyecta un radionúclido (a menudo un compuesto marcado con tecnecio-99m o talio-201) por vía intravenosa al alcanzarse el ejercicio máximo, después de lo cual se obtienen las imágenes. El radionúclido se acumula en proporción al grado de perfusión de las células miocárdicas viables. Por ende, las regiones con perfusión deficiente durante el ejercicio (es decir, las regiones con isquemia) no acumulan el radionúclido y aparecen en la imagen como focos fríos. Sin embargo, las regiones con infarto irreversible tampoco captan el radionúclido, por lo que también se aprecian como focos fríos.
Ecocardiografía de esfuerzo
Las pruebas de esfuerzo con imágenes ecocardiográficas constituyen otra técnica para diagnosticar la isquemia de miocardio en pacientes con alteraciones de base del segmento ST o la onda T, o en aquellos con resultados equívocos en la prueba estandarizada de esfuerzo.
La prueba revela la presencia de isquemia miocárdica inducible de desarrollarse en regiones ventriculares con disfunción contráctil tras el esfuerzo físico.
Pruebas de esfuerzo farmacológico
Para los pacientes incapaces de ejercitarse (p.ej., aquellos con artritis de la cadera o la rodilla) se pueden realizar pruebas de esfuerzo farmacológico con distintos agentes, incluidos vasodilatadores o inotrópicos. La estrategia más frecuente es recurrir a un vasodilatador coronario como la adenosina, el regadenosón o el dipiridamol. La adenosina y el regadenosón se unen a los receptores A 2ª de la adenosina en las células de músculo liso vascular, lo que genera vasodilatación coronaria.
Debido a que las regiones isquémicas muestran ya una vasodilatación máxima (para compensar las estenosis coronarias epicárdicas), la vasodilatación inducida por estos agentes incrementa el flujo hacia el miocardio irrigado por las arterias coronarias sanas y secuestra la sangre, alejándose de los segmentos enfermos.
La administración de estos agentes farmacológicos suelen aunarse a estudios de imagenología nuclear para identificar regiones miocárdicas con compromiso de la perfusión.
Angiografía coronaria
La estrategia más directa para identificar las estenosis arteriales coronarias es la angiografía coronaria, en que las lesiones ateroesclerosas se visualizan por medios radiográficos tras la inyección de un medio de contraste radiopaco en la arteria.
Aunque por lo general es seguro, el procedimiento se asocia con un riesgo bajo de complicaciones relacionado de manera directa con su naturaleza invasiva. Por esta razón, la angiografía coronaria suele reservarse para pacientes cuyos síntomas anginosos no responden de forma adecuada a la terapia farmacológica, para aquellos con un cuadro inestable, o cuando los resultados de las pruebas no invasivas muestran tal grado de anomalía que sea probable la existencia de una angina grave que justifique la revascularización.
Estudios de imagen no invasivos de las arterias coronarias
Se han desarrollado alternativas diagnósticas a la angiografía coronaria para visualizar por medios conservadores las arterias en cuestión. La angiografía coronaria mediante tomografía computarizada (ACTC) con administración de contraste intravenoso, permite visualizar estenosis mayores del 50% del lumen coronario, con una sensibilidad aproximada del 90% y una especificidad de 65 a 90%.
La ACTC se considera una alternativa a las pruebas de esfuerzo para facilitar la exclusión de angina significativa en pacientes con riesgo bajo o intermedio que acuden con dolor precordial inespecífico.
Historia natural
El paciente con angina crónica puede no mostrar cambios en el patrón estable de isquemia durante años. Sin embargo, en algunos individuos la evolución puede ir marcada por el desarrollo de angina inestable, infarto de miocardio o muerte súbita de origen cardíaco. Estas complicaciones a menudo se relacionan con la trombosis aguda en el sitio en que se daña una placa aterosclerosa.
La mortalidad asociada ha declinado en grado significativo durante las décadas recientes: la tasa de muerte ajustada con base en la edad ha caído más de 50%. Es probable que esto se relacione con la disminución del riesgo ateroescleroso mediante el mejoramiento del estilo de vida (p.ej., menor consumo de tabaco, menor consumo de grasas en la dieta y más ejercicio); mejoramiento de las estrategias terapéuticas y de la supervivencia tras los síndromes coronarios agudos y avances en las terapias farmacológicas y mecánicas.
RATAMIENTO
Tratamiento médico de episodio anginoso agudo
– Nitroglicerina sublingual
Tratamiento médico para la prevención de episodios isquémicos recurrentes
– Betabloqueadores adrenérgicos
– Nitratos orgánicos
– Antagonistas de los canales de calcio
Tratamiento médico para la prevención de eventos cardíacos agudos
– Tratamiento antiagregante (ácido acetilsalicílico)
– Antagonistas del receptor plaquetario (P2Y12 DEL ADP)
– Tratamiento para la regulación de los lípidos (estatinas)
– Inhibidores de la enzima convertidora de angiotensina
Revascularización
– Angioplastia coronaria transluminal percutánea
– Stents liberadores de fármacos
– Cirugía de revascularización coronaria
PATOGENIA DE LOS SÍNDROMES CORONARIOS AGUDOS
Más de 90% de los síndromes coronarios agudos deriva del daño a una placa aterosclerosa, con agregación plaquetaria subsecuente y formación de un trombo coronario. El trombo transforma una región de una placa estenótica en una oclusión grave o total, y el compromiso del flujo sanguíneo genera un desequilibrio marcado entre el aporte y la demanda miocárdicas de oxígeno.
Causas de infarto de miocardio
- Rotura de la placa ateroesclerosa con sobreposición de trombo
- Síndromes vasculíticos
- Embolia coronaria (p.ej., por endocarditis, válvulas cardíacas artificiales)
- Anomalías congénitas de las arterias coronarias
- Trauma o aneurisma coronario
- Disección espontánea de arteria coronaria
- Espasmo coronario intenso (primario o inducido por cocaína)
- Incremento de la viscosidad de la sangre (p.ej., policitemia vera, trombocitosis)
- Incremento marcado de la demanda miocárdica de oxígeno (p.ej., estenosis aórtica grave)
Alteraciones funcionales post-infarto de miocardio
- Compromiso de la contractilidad y la distensibilidad
- Remodelamiento ventricular
Complicaciones
- Isquemia recurrente
- Arritmias
-
- Fibrilación ventricular
-
- Arritmias supraventriculares
-
- Bloqueos de conducción
- Disfunción miocárdica
-
- Insuficiencia cardíaca
-
- Shock cardiogénico
- Infarto del ventrículo derecho
- Complicaciones mecánicas
-
- Rotura de músculos papilares
-
- Rotura de la pared libre del ventrículo
-
-
- Pseudoaneurisma
-
-
- Rotura del tabique interventricular
-
- Aneurisma ventricular verdadero
- Pericarditis
- Tromboembolia
Pasamos a exponer cuatro casos en los que la muerte súbita se produjo en el puesto de trabajo o dirigiéndose a él:
EXPOSICIÓN DE CASOS
CASO 1
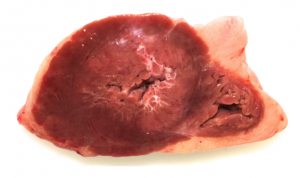
Autopsia nº 373-18
Hombre de 69 años, que murió mientras conducía su vehículo en dirección a su trabajo, saliéndose de la vía y encontrado en el arcén sin vida
Se desconocen antecedentes patológicos
Corazón: 550 g.
Trombosis coronaria en el tercio medio de la rama descendente anterior
Patrón de cardiopatía isquémica crónica
CASO 2
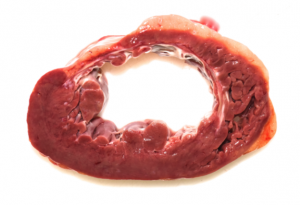
Autopsia nº 454-18
Hombre de 45 años, que falleció súbitamente en la vía pública mientras estaba descargando cajas de fruta
Antecedente patológico de stent en la descendente anterior
Corazón: 495 g.
Trombosis sobre el stent en el tercio proximal de la referida coronaria
Hallazgo de pseudoaneurisma de cara anterior del ventrículo izquierdo
CASO 3
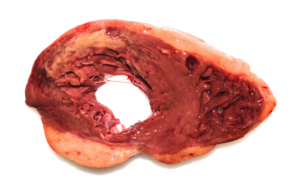
Autopsia nº 1814-18
Hombre de 64 años, camionero, hallado muerto en área de descanso de una gasolinera, mientras transportaba recambios de coche
Diabético en tratamiento con metformina y tabaquismo
Corazón: 740 g.
Trombosis en el tercio proximal de la rama descendente anterior
Diagnóstico de cardiopatía isquémica de 2-3 días de evolución en la cara anterior del ventrículo izquierdo; coronariopatía generalizada
CASO 4
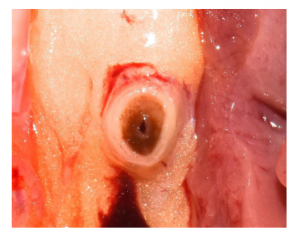
Autopsia nº 1020-18
Hombre de 66 años, que falleció mientras se hallaba trabajando en un concesionario de coches
Antecedente patológico de tabaquismo
Corazón: 435 g.
Trombosis coronaria en el tercio proximal de la rama derecha
Se ha constatado una cardiopatía isquémica reciente en un músculo papilar del ventrículo izquierdo y de etiología más antigua en la cara posterior del referido ventrículo
A continuación enumeramos diez SENTENCIAS, referentes a la contingencia de incapacidad o calificación de accidente laboral:
1 – TSJMU. Sala de lo Social: 2018: 1616
Profesión: Conductor
Enfermedad: Infarto agudo de micardio
Situación de IT deriva de contingencia laboral porque el infarto sufrido por el trabajador demandante fue durante el tiempo y lugar de trabajo
IT por contingencia de accidente laboral
2 – TSJC. Nº 647 2012
Profesión: Especialista textil
Enfermedad: Insuficiencia cardíaca con una fracción de eyección del 49%
Contingencia: Incapacidad Permanente Total
3 – TSJC. Nº 1924 2010
Profesión: Conductor
Enfermedad: Insuficiencia cardíaca con una FEVI del 43% e imposibilidad de revascularización completa
Contingencia: Incapacidad Permanente Total
4 – TSJC. Nº 5562 2009
Profesión: Conductor de transporte
Enfermedad: Patología cardíaca
Contingencia: Incapacidad Permanente Total
5 – TSJC. Nº 7016 2008
Profesión: Peón de la construcción
Enfermedad: Cardiopatía
Contingencia: Incapacidad Permanente Total
6 – TSJC. Nº 6883 2007
Profesión: No consta
Enfermedad: Cardiopatía valvular severa
Contingencia: Incapacidad Permanente Absoluta
7 – Sala Social del TS de 8-X-2009; recurso 1871/2008
Profesión: Categoría profesional de viajante
Enfermedad: IAM con resultado de muerte
Contingencia: Accidente laboral en misión
8 – TS. Sala de lo Social: 2017: 3072A
Profesión: Oficial de limpieza
Enfermedad: IAM con resultado de muerte
Contingencia: Accidente laboral
9 – TS. Sala de lo Social: 2018: 11578ª
Profesión: Jefe administrativo
Enfermedad: IAM con resultado de muerte
Contingencia: Accidente laboral
10 – TS. Sala de lo Social: 2013: 6543
Profesión: Oficial 1º siderometalúrgico
Enfermedad: Cardiopatía isquémica, IAM, stent
Contingencia: Accidente laboral. Incapacidad Per. Total
EVALUACIÓN DE LOS PACIENTES DESPUÉS DE UN INFARTO DE MIOCARDIO
A través de tres ítems, la clínica, la exploración física y pruebas de laboratorio.
Los parámetros básicos que se debe investigar son la existencia de disfunción ventricular izquierda y la presencia o no de isquemia residual.
Para ello se emplean métodos diagnósticos muy diversos, como son:
- Prueba de esfuerzo
- Ecocardiograma (reposo, esfuerzo, catecolaminas)
- Ventriculografía isotópica (reposo y esfuerzo)
- Monitorización con Holter (arritmias e isquemia silente)
- Gammagrafía miocárdica con Talio-201
- Coronariografía
- Estudio electrofisiológico
Factores de mal pronóstico tras el infarto agudo de miocardio a corto y medio plazo:
- Infarto agudo de miocardio de gran tamaño
- Disminución de la fracción de eyección ventricular < 40%
- Aumento del volumen telesistólico ventricular izquierdo
- Insuficiencia cardíaca congestiva
- Infarto agudo de miocardio de localización anterior
- Infarto agudo de miocardio previo
- Reinfarto o extensión del infarto
- Enfermedad arterial coronaria severa
- Oclusión permanente de la arteria culpable del infarto
- Angina postinfarto
- Prueba de esfuerzo anómala
- Fibrilación auricular y otras arritmias supraventriculares
- Bloqueo nuevo de rama del haz de His
- Bloqueo de segundo grado tipo Mobitz II o bloqueo cardíaco completo
- Fibrilación o taquicardia ventricular
- Extrasistolia compleja o frecuente
- Electrocardiograma de señal promediada anómalo
- Taquicardia ventricular monomórfica sostenida inducible durante el estudio electrofisiológico
- Edad avanzada
- Sexo femenino
- Diabetes Mellitus
- Hipertensión
- Tabaquismo continuado
- Niveles altos de colesterol
Capacidad funcional:
Se entiende la cantidad máxima de oxígeno, en litros por minuto, que un individuo puede llegar a consumir realizando ejercicio físico, representando el oxígeno transportado y utilizado en el metabolismo celular.
Un MET (o equivalente metabólico) es la unidad que representa el consumo de oxígeno promedio en condiciones basales y equivale al consumo de oxígeno de un individuo en situación de reposo (3,5 ml de oxígeno por Kg de peso y minuto). Por tanto, 6 METS es una actividad física que multiplica por seis ese consumo basal.
ACCIDENTE DE TRABAJO
Es un concepto jurídico y no médico. Sin embargo, como médicos podríamos definir el accidente como una “acción traumática, violenta, acaecida durante el trabajo y por efectos de éste, y cuya consecuencia es la muerte, la incapacidad o la enfermedad del trabajador”.
El artículo 156 de la Ley General de la Seguridad Social (LGSS) define el accidente de trabajo como “toda lesión corporal que el trabajador sufra con ocasión o por consecuencia del trabajo que ejecuta por cuenta ajena”.
Por lesión debemos entender no sólo los traumatismos, es decir, aquellos que se traducen en una lesión inmediata y como respuesta patológica directa a los agentes traumáticos, enormemente frecuentes en el ámbito laboral, sino también las enfermedades tanto somáticas, como psíquicas (incluyendo por ejemplo el estrés laboral, el síndrome del quemado o burn-out, etc.).
EL SISTEMA DE INCAPACIDADES EN EL SISTEMA NACIONAL DE SALUD
Incluyen:
- Incapacidad Temporal
- Incapacidad Permanente, clasificada en diversos grados:
-
- Parcial para la profesión habitual
– Supone una reducción > 33%
-
- Total para la profesión habitual
-
- Absoluta para todo tipo de trabajo
-
- Gran invalidez
CUANTIFICACION DE LA INCAPACIDAD
En la “Valoración de las discapacidades y del daño corporal (Louis Mélennec)” se han definido cinco grados de incapacidad funcional, que se corresponden con los cinco niveles de esfuerzo que se exponen a continuación:
Trastornos ligeros (grupo I)
La capacidad frente al esfuerzo es normal. El porcentaje de incapacidad está comprendido entre el 0 y el 5%.
Trastornos moderados (grupo II)
La capacidad de esfuerzo no es completamente normal, pero el paciente continúa siendo apto para realizar esfuerzos importantes o relativamente importantes. El porcentaje de incapacidad varía entre el 5 y el 15%.
Trastornos medios (grupo III)
La capacidad de esfuerzo está alterada, pero el paciente sigue siendo apto para realizar esfuerzos medios. El porcentaje de incapacidad estaría entre el 15 y el 30%.
Trastornos importantes (grupo IV)
La capacidad de esfuerzo está reducida o muy reducida, aunque el paciente continúa siendo apto para realizar esfuerzos moderados. El porcentaje de incapacidad oscila entre el 30 y el 60%.
Trastornos muy importantes (grupo V)
La capacidad de esfuerzo está muy disminuida. El porcentaje de incapacidad es superior al 60%.
DIVISIÓN DE LOS PACIENTES EN BAJO, MEDIO Y ALTO RIESGO
En base a la anamnesis, exploración física y pruebas cardiológicas invasivas y no invasivas realizadas al paciente, se puede estratificar a los pacientes en bajo, medio y alto riesgo de complicaciones tras el infarto.
Es evidente que los pacientes de alto riesgo como los que tienen angina grave, insuficiencia cardíaca descompensada o arritmias no controladas no son candidatos para que vuelvan a trabajar.
Bajo riesgo
Curso clínico sin complicaciones
Ausencia de signos de isquemia miocárdica residual
Capacidad funcional > 7 METS
Fracción de eyección > 50%
Ausencia de arritmias ventriculares severas
Riesgo medio
Presencia de angor de esfuerzo o isquemia a cargas mayores de 5 METS
Fracción de eyección entre 35-49%
Defectos reversibles con talio
Riesgo alto
Infarto previo. Insuficiencia cardíaca. Arritmias ventriculares malignas
Fracción de eyección < 35% en reposo
Capacidad funcional < 5 METS con respuesta hipotensiva o depresión del segmento ST > 1 mm.
Depresión del segmento ST > 2 mm a una frecuencia cardíaca inferior a 135 latidos por minuto
Respuesta hipotensiva al ejercicio
NATURALEZA DEL TRABAJO Y SUS EXIGENCIAS FÍSICAS
Para conocer cuál es la capacidad funcional del enfermo se realiza una ergometría (generalmente limitada por síntomas a las seis semanas después del infarto agudo de miocardio), haciéndonos una idea aproximada de cuál va a ser el rendimiento del paciente en una ocupación laboral y en la vida cotidiana. Los pacientes no elegibles para prueba de esfuerzo en razón de angina grave, insuficiencia cardíaca descompensada, o arritmias no controladas no son candidatos para entrenamiento físico ni para vuelta al trabajo.
Estos niveles promedio de MET para diversas ocupaciones resultan muy generales, pues van a depender de la velocidad con la que se efectúa el trabajo, la ciencia del trabajador y otros condicionantes que operen en el lugar de tarea (temperatura, estrés psicológico, etc.). En casos límite y dudosos, puede llegar a ser necesario permitir que el paciente retorne al trabajo y luego monitorizar la frecuencia cardíaca y respuesta del segmento ST durante la tarea. Alternativamente, estos parámetros pueden monitorizarse durante la realización de un trabajo simulado.
Cualquier trabajo que requiera hasta un 50-60% de la energía máxima desarrollada en la prueba de esfuerzo, el paciente lo podrá realizar sin problemas. En principio, un paciente que ha tenido un infarto agudo de miocardio, que se le hace una prueba de esfuerzo y alcanza 8-12 sin problemas, se le puede aconsejar perfectamente un trabajo que le suponga 6-7. Si la actividad laboral va a tener una duración en torno a ocho horas diarias, es preciso establecer un margen de seguridad, de tal manera que los gastos energéticos de ésta no deberían sobrepasar el 40% de la capacidad calculada en la ergometría.
Antes de que el paciente retorne al trabajo tenemos que tener claras las exigencias físicas del mismo, así como el ambiente en que el trabajo se desarrolla. Si el trabajo tiene sólo uno o dos aspectos que lo hacen muy agotador, puede que una simple modificación de la tarea o el apoyo de sus compañeros de trabajo o la ayuda de aparatos mecánicos lo hagan más soportable.
De todas formas, en todos los pacientes están desaconsejadas la realización de esfuerzos físicos de carácter violento, el estrés emocional intenso y la exposición brusca al frío. Estas situaciones pueden desencadenar angor incluso en pacientes asintomáticos en los que la ergometría muestra una buena capacidad funcional.
El antecedente de un infarto de miocardio en nuestro país supone un impedimento legal para la obtención y renovación de los permisos de conducir de las clases B.2, C.1, C.2, D y E, al tiempo que también es motivo de descalificación para pilotar.
Es importante conocer que la gran mayoría de los pacientes postinfarto podrían en un par de meses, e incluso en menos (dependiendo de la severidad del mismo ), volver a su actividad laboral. Sin embargo, la gran mayoría no lo hace por problemas sociolaborales ajenos a su situación física. La reincorporación o no al trabajo depende de la severidad del infarto, de la persistencia de la angina, de su función ventricular, de la edad, de su capacidad funcional y en definitiva de la estratificación del paciente en alto, medio o bajo riesgo.
En base a los datos de la prueba de esfuerzo podremos aconsejar o no la vuelta al trabajo en función de los gastos energéticos teóricos de cada profesión, de acuerdo a la tabla que muestra los consumos energéticos de distintas profesiones y actividades de tiempo libre. Para las actividades que puedan suponer esfuerzos físicos importantes de forma continuada, es preciso establecer un margen de seguridad, desaconsejándose actividades cuyos requerimientos energéticos superen el 40% del gasto energético alcanzado en la ergometría.
CONCLUSIONES
Hasta hace poco, la Jurisprudencia venía entendiendo que cualquier dolencia patológica de carácter cardíaco podía tener su origen en el ámbito laboral, lo que implicaba el reconocimiento prácticamente automático de este tipo de dolencias como accidente de trabajo.
En cambio en los últimos años, esto ha ido paulatinamente cambiando y ha ido endureciéndose la permisividad jurídica en las resoluciones judiciales, que resuelven la determinación de contingencia de este tipo de dolencias y para ello, estamos frente a unos cambios que presenta la Jurisprudencia.
Ha establecido criterios más rigurosos a la hora de determinar las circunstancias que rodean al trabajador víctima de estas enfermedades, así como de todas las causas que puedan influir en su desencadenamiento. Ejemplo de ello, existen varias sentencias, en que el juzgador parece limitar la calificación masiva de accidentes de trabajo y enfermedades profesionales en este tipo de dolencias cardíacas, todo ello sin olvidar que nos encontramos ante una materia muy casuística en que la más mínima circunstancia puede y debe ser tenida en cuenta.
Sabiendo que el significado de Accidente de Trabajo, es un concepto jurídico y no médico, los facultativos podríamos definir el Accidente como “una acción traumática y violenta, acaecida durante el trabajo y por efectos de éste y cuya consecuencia es la muerte, la incapacidad o la enfermedad del trabajador”.
El artículo 156 de la Ley General de la Seguridad Social (LGSS) define el Accidente de Trabajo como “toda lesión corporal que el trabajador sufra con ocasión o por consecuencia del trabajo que ejecuta por cuenta ajena”.
En lo referente a –ocasión- parece referirse a una aparición inmediata y por –consecuencia- que pueda diferir en el tiempo.
La Organización Internacional del Trabajo (OIT), destacó una serie de características que debía reunir la acción para considerarla Accidente de Trabajo, para diferenciarla de otras enfermedades ligadas también al trabajo y que son las siguientes:
- Por su origen: imprevisto y repentino
- Por su naturaleza: variable, no pudiéndose predecir su alcance, ni las consecuencias que se puedan derivar de él
- Por su patogenia: puede precisarse y medirse en el momento en que se produjo y cuando se inició la lesión
- La muerte o la lesión resultan de un hecho único, el traumatismo
A la vista de lo anteriormente explicitado, debemos entender que según la Real Academia de la Lengua, “lesión” es daño o detrimento corporal por herida, golpe o enfermedad.
A nuestro entender la “lesión corporal”, no sólo son los traumatismos, es decir aquellos que se traducen en una lesión inmediata y como respuesta patológica directa a los agentes traumáticos en el ámbito laboral, sino también las enfermedades (diferidas en el tiempo) tanto somáticas y psíquicas, como el estrés laboral, el “síndrome del quemado” y otros.
Según la Sentencia del Tribunal Supremo de 17 de junio de 1903, “el concepto de accidente incluye también el de enfermedad”.
El accidente de trabajo como contingencia protegida, se extendió también a los trabajadores por cuenta propia, mediante la Ley 53/2002 de 31 de diciembre (art.40.4), desarrollada por el RD 1273/2003 de 10 de octubre, que dio una nueva definición de accidente para los trabajadores autónomos.
El apartado 2º del artículo 3 reproduce las mismas circunstancias para tener la condición de accidente que el artículo 156 de la LGSS, con la única excepción del accidente “in itinere”, que solamente se reconoce a los autónomos dependientes. Todo ello, con la condición indispensable que el autónomo se haya acogido a la cobertura de incapacidad temporal.
A tenor del artículo 115.3 de la LGSS, según el cual se presumirá, salvo prueba de lo contrario, que “son constitutivos de accidente de trabajo, las lesiones que sufra el trabajador durante el tiempo y en el lugar de trabajo”.
Otros accidentes considerados como laborales, serían: Accidente “in itinere”, desempeño de cargas sindicales, tareas distintas a su categoría (actos de salvamento), enfermedad causada por el trabajo, enfermedades agravadas por el accidente, consecuencias modificadas por enfermedad, imprudencia profesional, culpabilidad civil o criminal del empresario o del compañero.
Por ello, el juego de la presunción exigirá que se acredite la ruptura del nexo causal lo que “se hace difícil en los casos de dolencias cardíacas, las cuales no son extrañas a las causas de carácter laboral”. El nexo causal no se “rompe”, lo que se valora es la acción del trabajo como factor desencadenante de una crisis … y esta posible acción del trabajo… No puede quedar excluida sólo por la prueba de que la enfermedad se padecía antes” (STS/4ª de 20 de octubre de 2009; rcud.1810/2008).
Para qué el infarto no se considere accidente laboral, la carga de la prueba corresponde al INSS, TGSS, Mutua, Servicio Público de Salud o empresa y se debe centrar en demostrar que NO existe nexo causal entre el infarto y el trabajo, bien porque se trate de enfermedad que por su propia naturaleza descarta o excluya la acción del trabajo como factor determinante o desencadenante, bien porque se aducen hechos que desvirtúen dicho nexo causal, lo que sucederá con facilidad en los supuestos de enfermedades en los que el trabajo no tuviera influencia, pero se hace difícil en los casos de dolencias cardíacas, las cuales no son extrañas a las causas de carácter laboral.
El Tribunal Supremo avisa en su Sentencia de 8 de marzo de 2016, que romper el nexo causal infarto de miocardio – accidente laboral “se hace difícil en los casos de las lesiones cardíacas”.
En resumen, “la presunción no se excluye porque se haya acreditado que el trabajador padeciera la enfermedad con anterioridad o porque se hubieran presentado síntomas antes de iniciarse el trabajo, porque lo que se valora a estos efectos no es, desde luego la acción del trabajo como causa de la lesión cardíaca, lo que no sería apreciable en principio dada la etiología común de este tipo de lesiones”.
Lo que se valora es la acción del trabajo en el marco del art. 115.2 f. LGSS, como factor desencadenante de una crisis, que es la que lleva a la situación de necesidad protegida; y esta posible acción del trabajo se beneficie de la presunción legal del art. 115.3 y no puede quedar excluida sólo por la prueba de que la enfermedad se padecía ya antes, pues aunque así fuera, es la crisis y no la dolencia previa la que hay que tener en cuenta a efectos de protección (STS/4ª de 27 de septiembre de 2007 rcud. 853/2006).
Dicho esto, se puede concluir, que las patologías cardíacas, síndromes coronarios agudos, cardiopatías isquémicas, valvulopatías y otras lesiones cardíacas, que sean calificadas de accidente laboral o tributarias de incapacidades laborales, deben cumplir los requisitos exigidos de laboralidad, es decir que ocurran en tiempo y en el lugar de trabajo.
Sobre los antecedentes personales de la enfermedad, citando Jurisprudencia, concluye que es irrelevante tenerlos, “ya que está expresamente prevista la calificación laboral en los supuestos de enfermedades o defectos padecidos con anterioridad, que se agraven como consecuencia de la lesión constitutiva de accidente (artículo 115.2 f LGSS).
Y queda remarcado… que es la crisis y no la dolencia previa, la que hay que tener en cuenta a efectos de protección.
Como epílogo al presente trabajo, reseñar que a nivel cardíaco es el infarto agudo de miocardio, que como tal genera una lesión en el músculo el que se considera accidente de trabajo, no así los cuadros de isquemia, en los cuales no existe lesión, siendo en la inmensa mayoría de casos, reversible.
BIBLIOGRAFIA
- ASPECTOS MEDICOLEGALES DE LA MUERTE SUBITA CARDIACA. Josep Castellá García. Jordi Medallo Muñiz. Teresa Marrón Moya. Revista Española de Cardiología. 2011
- AUTOPSIA CARDIACA EN PATOLOGIA FORENSE. Benito Morentín-Campillo. María Paz Suárez-Mier. Beatriz Aguilera-Tapia. Revista Española de Medicina Legal. 2013
- ASPECTOS MEDICO-FORENSES DE LA MUERTE SUBITA DEL ADULTO. Josep Castellà-García. Juan Carlos Borondo-Alcázar. Antonia Bertomeu-Ruiz y José Manuel Tortosa-López. Medicina Clínica. 2006
- CARDIOLOGIA. Bases fisiopatológicas de las cardiopatías. 6ª edición. Leonard S. Lilly. Wolters Kluwer
- PATOLOGIA ESTRUCTURAL Y FUNCIONAL. Robbins y Cotran. 9ª edición. Elsevier
- CARDIAC PATHOLOGY. S.Kim Suvarna. 2013. Springer
- AUTOPSY PATHOLOGY. Andrew J. Connolly. Walter E. Finkbeiner. Philip C. Ursell. Richard L.Davis. Third Edition. 2016. Elsevier
- LA MUERTE SUBITA. Oswald Londono. 2015. Minsk
- THE HOSPITAL AUTOPSY. Julian L. Burton. Guy N. Rutty. Third Edition. 2010. Hodder Arnold
- ANATOMIA PATOLOGICA ESPECIAL. Horacio Oliva Aldamiz. 2004. Ergon
- FORENSIC PATHOLOGY. David Dolinak. Evan Matshes. Emma Lew. 2005. Elsevier
- HISTOPATOLOGIA FORENSE. Manuel Salguero Villadiego. José Blanco Pampín. 2015. Ministerio de Justicia
- ESTRATIFICACION PRONOSTICA DESPUES DEL INFARTO DE MIOCARDIO. PREVENCION SECUNDARIA Y REHABILITACION. IAM. SECCION DE CARDIOPATIA ISQUEMICA DE LA SOCIEDAD ESPAÑOLA DE CARDIOLOGIA. 1994. E. Martín Huerta, V. Valle Tudela, M. Abeytúa y colaboradores
- SOCIEDAD ESPAÑOLA DE CARDIOLOGIA. NORMAS DE ACTUACION CLINICA EN CARDIOLOGIA
- FACTORES DE RIESGO EN ENFERMEDADES CORONARIAS Y REHABILITACION CARDIACA. LA PRACTICA DE LA CARDIOLOGIA. Hospital General de Massachusetts. 2ª Edición. 1991. Editorial Panamericana
- POSITION REPORT ON CARDIAC REHABILITATION: RECOMMENDATIONS OF THE AMERICAN COLLEGE OF CARDIOLOGY. JOURNAL OF THE AMERICAN COLLEGE OF CARDIOLOGY. 1986
- CARDIOPATIA ISQUEMICA: INFARTO DE MIOCARDIO. Juan Ramón Bley y Esther Pérez David. Servicio de Cardiología. Hospital General Universitario Gregorio Marañón de Madrid.





